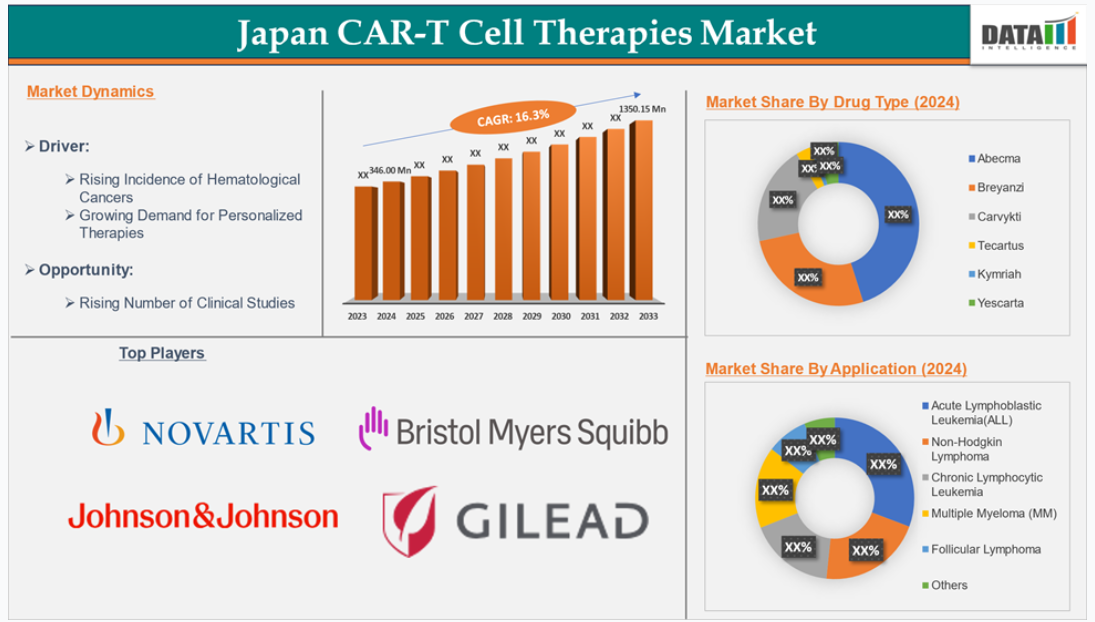
市場動向:推進要因と抑制要因
血液がんの発生率の上昇
日本における多発性骨髄腫、白血病、リンパ腫などの血液がんの発生率の上昇は、同国の CAR-T 細胞療法市場の成長を大幅に促進すると予想されます。日本の人口の高齢化が進む中、これらの血液関連がんの有病率は着実に増加しており、高度で効果的な治療法の必要性が高まっています。例えば、国際がん研究機関(IARC)のデータを参照すると、2022年に日本で報告された多発性骨髄腫の新規症例数は約6,988件でした。2025年までにこの数は7,350件に達すると予測されています。また、2030年までに日本の多発性骨髄腫の発生率は7,535件に達すると推計されています。
従来型の治療法は、再発例や難治性例では効果が限定的な場合が多く、CAR-T 細胞療法のような革新的な治療法の需要が高まっています。この最先端の治療法は、患者の免疫細胞を再プログラムしてがん細胞を標的とし、破壊するものであり、標準的な治療法を尽くした患者に新たな希望をもたらしています。意識の高まりと規制支援の強化が進む中、CARVYKTIの承認など最近の動向を背景に、日本はアジア太平洋地域におけるCAR-T細胞療法の主要市場となる可能性があります。したがって、上記の要因が市場成長を後押ししています。
治療費の高額
CAR-T 細胞療法は治療費が高額であるため、患者や医療制度の利用しやすさや手頃な価格に制限があり、市場の成長を大きく妨げています。特に、包括的な保険償還制度がない国では、治療費の高さが患者の利用を制限し、この治療法の市場浸透を妨げています。多くの医療提供者や保険会社は、長期的な費用対効果に関するデータがないことを理由に、CAR-T 細胞療法の保険適用を躊躇しており、その臨床的有効性にもかかわらず、この治療法の採用が制限されています。
市場セグメント分析
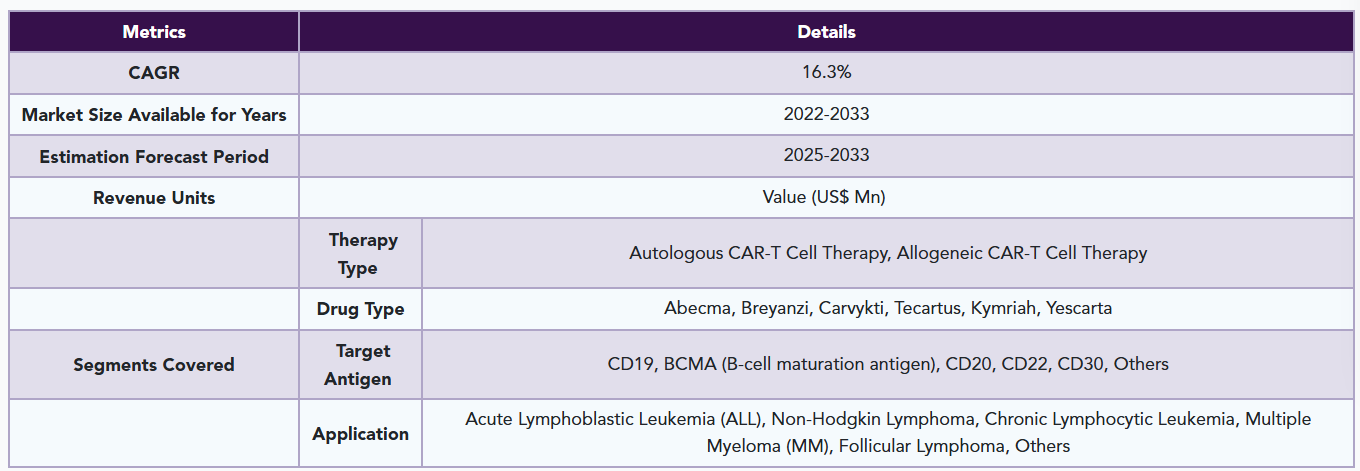
日本の CAR-T 細胞療法市場は、治療の種類、薬剤の種類、標的抗原、および用途に基づいて分類されています。
用途セグメントでは、多発性骨髄腫が CAR-T 細胞療法市場を支配すると予想されています。
多発性骨髄腫は、がん患者の増加、主要業界関係者による承認と発売活動の増加を背景に、日本の CAR-T 細胞療法市場の用途セグメントを牽引すると予想されています。例えば、2022年9月、生命を脅かす疾患向けの革新的な療法の開発、製造、商業化に注力するグローバルなバイオテクノロジー企業であるLegend Biotech Corporationは、日本の厚生労働省(MHLW)がCARVYKTI(ciltacabtagene autoleucel)の承認を付与したと発表しました。このBCMA標的CAR-T細胞療法は、再発または難治性の多発性骨髄腫の成人患者に対する治療薬として承認されました。
さらに、2023年12月、ブリストル・マイヤーズ スクイブ社のidecabtagene vicleucelが、少なくとも2つの前治療を受けた再発または難治性の多発性骨髄腫患者を対象に、日本で承認されました。この承認は、標準療法と比較して無増悪生存期間と客観的奏効率に有意な改善を示した第3相KarMMA-3試験の結果に基づいて行われました。
これらの進展は、日本のCAR-T療法市場における多発性骨髄腫への注目が高まっていることを示しています。承認されたCAR-T療法の可用性が増加することで、有効な療法に対する需要の増加に対応し、多発性骨髄腫がこの市場セグメントにおける主要な適応領域として確立されることが期待されます。
市場プレイヤー
CAR-T細胞療法市場の主要企業には、Gilead Sciences, Inc., Bristol Myers Squibb Company, Johnson & Johnson Services, Inc., Novartis AGなどが挙げられます。
主要な動向
- 2024年4月、ジョンソン・エンド・ジョンソンは、米国食品医薬品局(FDA)が、CARVYKTI (ciltacabtagene autoleucel;cilta-cel)を、プロテアソーム阻害剤と免疫調節剤を含む少なくとも1つの前治療を受けた後、レナリドミドに耐性のある再発または難治性多発性骨髄腫の成人患者に対する治療薬として承認したと発表しました。
- 2024年1月、ブリストル・マイヤーズ スクイブは、Breyanzi(lisocabtagene maraleucel)について、米国食品医薬品局(FDA)および日本の厚生労働省(MHLW)から3件の規制当局の承認を取得したと発表しました。
- 2023年4月、タカラバイオ株式会社は、カナダ保健省に臨床試験申請(CTA)を提出し、CD19 JAK/STAT CAR-T療法(TBI-2001)のフェーズI/Ib臨床試験を開始するための「異議なし書簡」を受領しました。必要な手続きが完了次第、CD19陽性B細胞リンパ腫患者を対象とした研究者主導の臨床試験が開始されます。
このレポートを購入する理由
- パイプラインとイノベーション:進行中の臨床試験、製品パイプラインをレビューし、今後の医薬品の進歩を予測します。
- 種類のパフォーマンスと市場での位置付け:製品のパフォーマンス、市場での位置付け、成長の可能性を分析し、戦略を最適化します。
- 実世界でのエビデンス:患者のフィードバックとデータを製品開発に統合し、成果の向上を図ります。
- 医師の好みと医療制度への影響: 医療提供者の行動、および医療システムの統合が採用戦略に与える影響を検証します。
- 市場の最新情報および産業の変化:最近の規制の変更、新しい政策、および新興技術を網羅しています。
- 競争戦略:競合他社の戦略、市場シェア、および新興企業を分析します。
- 価格設定および市場アクセス:価格設定モデル、償還の傾向、および市場アクセス戦略をレビューします。
- 市場参入および拡大:新しい市場への参入およびパートナーシップの構築に最適な戦略を特定します。
- サプライチェーンの最適化:サプライチェーンのリスクと、効率的な種類配送のための流通戦略を評価します。
- サステナビリティと規制の影響:医療分野におけるエコフレンドリーな取り組みと規制の動向に焦点を当てます。
- 市販後調査:市販後のデータを用いて、製品の安全性とアクセス性を向上させます。
- 薬事経済学と価値に基づく価格設定:研究開発における価値に基づく価格設定とデータに基づく意思決定への移行を分析します。
日本 CAR-T 細胞療法市場レポートには、約 42 の表、33 の図、180 ページが含まれます。
2024 年のターゲットオーディエンス
製造業者:製薬会社、バイオテクノロジー企業、受託製造業者、流通業者、病院
規制および政策:コンプライアンス担当者、政府、医療経済学者、市場アクセス専門家
技術およびイノベーション:研究開発担当者、臨床試験マネージャー、医薬品安全性監視の専門家
投資家:医療投資家、ベンチャーファンド投資家、製薬マーケティングおよび販売
コンサルティングおよびアドバイザリー:医療コンサルタント、業界団体、アナリスト
サプライチェーン:流通およびサプライチェーンマネージャー
消費者および支援団体:患者、支援団体、保険会社、学術および研究:学術機関
- 市場紹介と範囲
- 本レポートの目的
- レポートの対象範囲と定義
- レポートの範囲
- 経営陣の洞察と重要なポイント
- 市場のハイライトと戦略的ポイント
- 主な傾向と将来予測
- 治療の種類別スニペット
- 薬剤の種類別スニペット
- 標的抗原別スニペット
- 用途別スニペット
- ダイナミクス
- 影響要因
- 推進要因
- 血液がんの発生率の上昇
- 個別化治療に対する需要の高まり
- XX
- 制約
- 治療費の高額
- 厳格な規制の枠組み
- XX
- 機会
- 臨床試験数の増加
- XX
- 影響分析
- 推進要因
- 影響要因
- 戦略的洞察と産業の見通し
- 市場リーダーと先駆者
- 新興の先駆者と有力企業
- 最大売上のブランドを持つ確立されたリーダー
- 確立された製品を持つ市場リーダー
- CXO の見解
- 最新動向とブレークスルー
- ケーススタディ/進行中の研究
- 北米規制および償還の状況
- ポーターの 5 つの力分析
- サプライチェーン分析
- 特許分析
- SWOT 分析
- アンメットニーズとギャップ
- 市場参入および拡大のための推奨戦略
- シナリオ分析:ベストケース、ベースケース、およびワーストケースの予測
- 価格分析および価格動向
- 主要オピニオンリーダー
- 市場リーダーと先駆者
- CAR-T 細胞療法市場、治療の種類別
- はじめに
- 市場規模分析および前年比成長率分析(%)、治療の種類別
- 市場魅力度指数、治療の種類別
- 自家 CAR-T 細胞療法*
- はじめに
- 市場規模分析および前年比成長率分析(%)
- 同種 CAR-T 細胞療法
- はじめに
- CAR-T 細胞療法市場、薬剤の種類別
- 概要
- 市場規模分析および前年比成長率(%)、薬剤の種類別
- 市場魅力度指数、薬剤の種類別
- アベクマ*
- 概要
- 市場規模分析および前年比成長率(%)
- ブレヤンジ
- カーヴィクティ
- テカルタス
- キムリア
- イェスカ
- 概要
- CAR-T 細胞療法市場、標的抗原別
- 概要
- 市場規模分析および前年比成長率分析(%)、標的抗原別
- 市場魅力度指数、標的抗原別
- CD19*
- 概要
- 市場規模分析および前年比成長率分析(%)
- BCMA(B細胞成熟抗原)
- CD20
- CD22
- CD30
- その他
- 概要
- CAR-T細胞療法市場、用途別
- 概要
- 市場規模分析および前年比成長率分析(%)、用途別
- 市場魅力度指数、用途別
- 急性リンパ性白血病(ALL)*
- 概要
- 市場規模分析および前年比成長率分析(%)
- 非ホジキンリンパ腫
- 慢性リンパ性白血病
- 多発性骨髄腫(MM)
- 濾胞性リンパ腫
- その他
- 概要
- 競争環境と市場ポジション
- 競争概要と主要市場プレイヤー
- 市場シェア分析とポジショニングマトリックス
- 戦略的提携、合併・買収
- 製品ポートフォリオとイノベーションの主要動向
- 企業ベンチマーク
- 企業プロファイル
既存企業
- Gilead Sciences, Inc.
- 会社概要
- 製品ポートフォリオ
- 製品
- 製品 KPI
- 過去および予測製品売上高
- 製品販売数量
- 製品ポートフォリオ
- 会社概要
- 財務概要
- 会社収益
- 地域別収益構成
- 収益予測
- 主な動向
- 合併および買収
- 主な製品開発活動
- 規制当局の承認など
- SWOT 分析
- 地域別収益構成
- ブリストル・マイヤーズ スクイブ社
- ジョンソン・エンド・ジョンソン・サービス社
- ノバルティス社
- 会社収益
新興企業
- タカラバイオ株式会社
リストは完全ではありません
- 仮定および調査方法
- データ収集方法
- データ三角測量
- 予測手法
- データの検証および妥当性確認
- 付録
- 弊社およびサービスについて
- お問い合わせ
*** 免責事項 ***
https://www.globalresearch.co.jp/disclaimer/